生徒たちの「分からない」を取り上げて考えていきます。
解き方が分からない前提で「どんな風に考えて解いていくか」という過程を書いていくので、ぜひご自身でも解き方を考えながら読み進めてみてください。
今回は、とある中学の授業で出されたプリントからの出題、理科(2年、化学) の問題です。
問題

今回から、記事の構成や書き方をこれまでとは変えて、できるだけシンプルに、なるべく短く、を心がけて書いていきます。
(1)
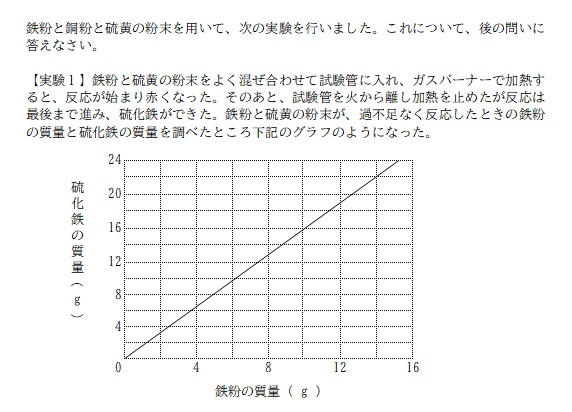
グラフから必要な情報を読み取ります。
縦線と横線の交点をグラフが通る場所を探すと、鉄粉 14g / 硫化鉄 22g であることが分かる。
そこから反応した硫黄の質量を求めると、22-14=8 で、硫黄 8g となる。
これらの情報から3つの物質の質量比を求めると、
鉄:硫黄:硫化鉄 = 14:8:22
= 7:4:11
となる。あとはこの比率を利用して硫化鉄 16.5g に対する硫黄の質量を求めれば良い。
硫黄:硫化鉄
4:11 = x:16.5
11x = 66
x = 6
A. (1) 6.0g
(2)
この問題も (1) で使った「鉄/硫黄/硫化鉄」の比率を使って解くことができる。
気を付けるポイントは、鉄粉 26.8g が全て反応したのか、一部が反応し余りが出たのか、という点。もちろん、硫黄 12.0g について同様に考えても良い。
ここの意味が分かっていないと 26.8+12.0=38.8g の硫化鉄!みたいな間違った回答をすることになる。
ますは、鉄粉 26.8g が完全に反応するのに必要な硫黄の質量を考えてみる。
鉄:硫黄
7:4 = 26.8:x
7x = 107.2
x = 15.3・・・
となるので、鉄粉 26.8g が完全に反応するには硫黄 12.0g だけだと少し足りないことが分かる。言い方を変えると、この硫黄の量では鉄粉は全て反応せず余る、ということ。
つまり、鉄粉 26.8g が全て反応して何g の硫化鉄になるか、ではなく、硫黄 12.0g が全て反応して何g の硫化鉄になるか、を考えれば良い。
硫黄:硫化鉄
4:11 = 12:x
4x = 132
x = 33
A. (2) 33.0g
(3)
実験2の問題文に書いてある、銅と硫化銅の質量から反応した硫黄の質量を求め、それらの情報から3者の質量の比率を求める。
硫化銅 5.1 - 銅 3.4 = 硫黄 1.7
銅:硫黄:硫化銅 = 3.4:1.7:5.1
= 2:1:3
銅の原子と硫黄の原子が1:1で結びつく、と記載があるので上記の質量比率がそのまま原子1個の質量比率となることが分かる。
問題 (1) で求めた鉄/硫黄/硫化鉄の質量比率、
鉄:硫黄:硫化鉄 = 7:4:11
これも上記の質量比率がそのまま原子1個の質量比率となる。問題文を読んでも鉄の原子と硫黄の原子の結びつきが1:1という記述はないが、硫化鉄の化学反応式「Fe+S→FeS」を知っていれば考えることができる。
ここまでで、銅と硫黄、鉄と硫黄、それぞれの原子1個の質量比率が分かったが、銅と鉄の質量比率を求めるには2つの比率の中で共通する硫黄の比率を揃えて比較する必要があるので、
鉄:硫黄 = 7:4
銅:硫黄 = 2:1 ← こっちを 4倍して硫黄の比率を揃える
鉄:硫黄 = 7:4
銅:硫黄 = 8:4
よって、鉄の原子1個と銅の原子1個の質量の比は 7:8 となる。
A. (3) 7:8
(4)
鉄と硫化鉄、銅と硫化銅、それぞれの比率を元に考える。
鉄:硫化鉄 = 7:11
銅:硫化銅 = 2:3
硫黄については「十分な量を混ぜ」と記載があるので、特に考える必要はないです。上記比率をそのまま質量と考え、鉄粉と銅粉の混合物が 20g、硫化鉄と硫化銅の混合物が 31g になるように考える。
鉄+銅が 20g (偶数) ということは、鉄 (奇数) + 銅 (偶数) という組み合わせにはならないことが分かる。銅は何倍しても偶数なので、鉄の方を偶数にするよう考える。
鉄が 7 の 4倍だと 28 となり問題文の 20g を超えてしまうので使えるのは 2倍の 14g しかないと考えることができる。そこに銅を加えて 20g にするには、銅 2 を 3倍して足せば良い。
鉄:硫化鉄 = 7:11 ← 2倍
銅:硫化銅 = 2:3 ← 3倍
鉄:硫化鉄 = 14:22
銅:硫化銅 = 6:9
これで混ぜ合わせると、
鉄+銅:硫化鉄+硫化銅 = 20:31
となり問題文と合致する質量を求めることができましたね。よって鉄と銅の混合物の中の鉄の質量は 14g であると分かります。
A. (4) 14.0g
いかがでしたか?
私だったらこんな風に考えて解くかな、という解説です。他にも解き方、考え方はいろいろあると思います。そういうのを考えたり調べて勉強するのも面白いかもしれません。
特別な化学の知識がないと解けない、というような問題ではなく、問題の中の情報を整理し考えれば解ける問題だと思います。個人的にはこういう「考えれば解ける問題」は好きですね。
-----
問題を解けば終わり、答えが分かれば終わり、ではなく、問題を解く過程でたくさんの「なんだろう?」っていう疑問を見つけて、それを理解していく努力が勉強です。
そしてその「なんだろう?」を解き明かしたときの達成感を味わうのが勉強の醍醐味です!
ぜひたくさんの「分からない」を見つけて、それを「分かった!」に変えていく努力をしていってくださいね!
以上です。お疲れさまでした!
(*ᴗˬᴗ)⁾⁾








コメントをお書きください
あ (月曜日, 28 10月 2024 09:27)
あ